Battery Boot Camp (part I)
Hello 大家好,欢迎来到小明的自习室,我是爱学习的小明。录这个视频主要是想在学习电池知识的同时做做笔记,以便加深映像;另外也算抛砖引玉,希望和行业内的小伙伴交流讨论,大家共同进步。
那么,首先我来做一下简单的自我介绍:本人于2009年进入吉林大学化学院学习,2013年本科毕业后进入物理学院的电池实验室攻读硕士学位,期间从事二维电池材料的研究,然后在2016年毕业加入宁德时代,从事动力电池的开发工作;在经历了大厂的洗礼后,先后于2018年秋天和2022年春天分别加入大众汽车和华人运通,从整车厂视角开发电池;今年春天来到了目前就职的柯锐世,从事车用低压电池的开发。
从2013到2023,接触电池10年来也积累了一些经验和感悟,希望通过视频的方式得以保留,并分享给同路人。
OK,下面介绍下视频内容的来源及作者:这篇笔记主要围绕左边这本书《Battery Modeling》展开,是一本介绍电池管理系统基础知识的书,它的作者是右边这位叫Gregory的教授,他目前就职于科罗拉多大学的电气与计算机工程学院,大家如果有兴趣可以访问Gregory教授的大学主页,里面有更详尽的研究课题介绍和实验室简介。这本书不仅深入浅出地介绍了电池的物理化学特性和建模规则,并且很良心地分享了建模基础数据和模型代码,方便读者练习和模拟,我也会将书籍和相关资料下载链接放在视频结尾,以便大家取用。讲述地过程中如有错误或疑问,请大家在视频下方留言给我,我会及时改正和答复。
那么,下面介绍下本书的主要章节:分别是第一章 电池训练营,第二章 等效电路模型,第三章 微尺度电芯模型,第四章 连续尺度电芯模型,第五章 状态空间模型与离散时间实现算法,第六章 降阶模型,以及最后一章 热学建模。本期为第一期视频,我们来介绍第一章 电池训练营。
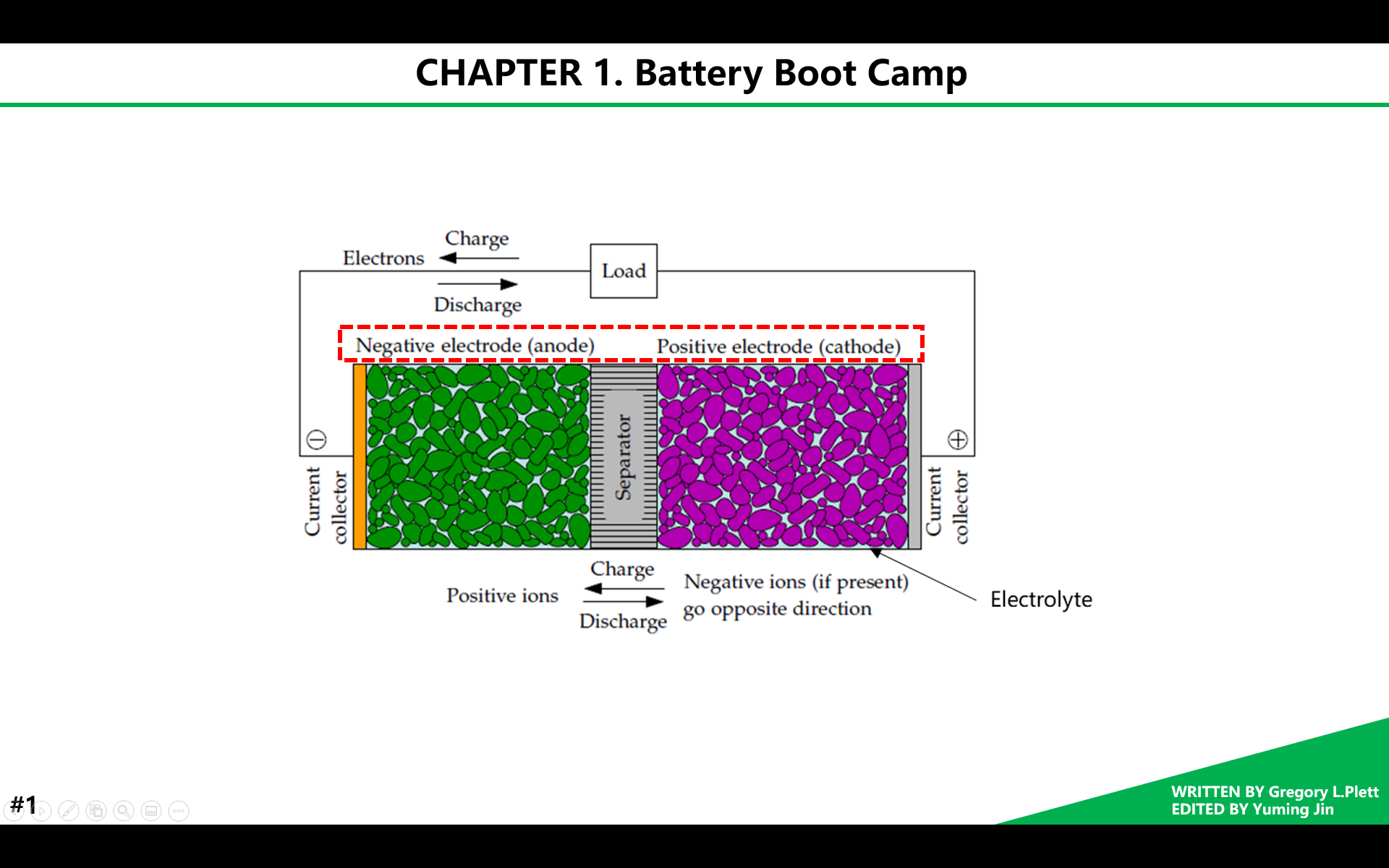
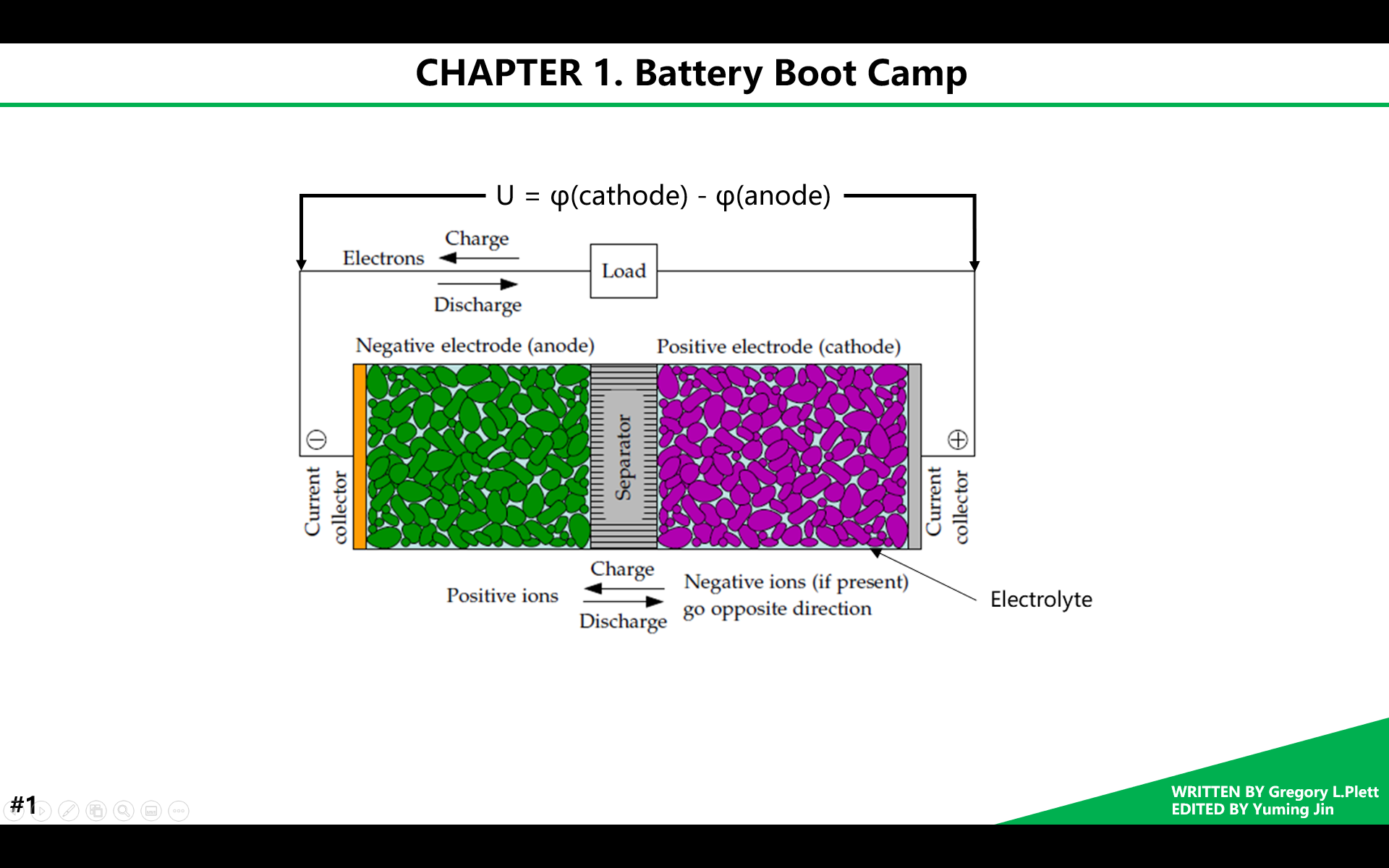
单体电池通常由一些主要零部件组成,包括:负极、正极、电解液和隔离膜,其中正负极通常包含集流体。在电化学电池中,负极通常是纯金属,或合金,甚至是氢气,例如汽车的12V铅酸电池的负极是纯金属铅。电池放电时,负极释放电子到外电路,负极表面发生氧化反应;充电时,负极从外电路接收电子,被还原。因此电化学电池中的反应也被称为氧化还原反应。负极也经常被称为阳极,即发生氧化反应的电极,但注意,只有在电池充电时属于这种情况。在电化学电池中,正极通常是金属氧化物、硫化物或氧气,例如铅酸电池的正极是氧化铅。放电时,正极从外电路接收电子,被还原;充电时,正极释放电子到外电路,发生氧化反应。正极通常被叫做阴极,即发生还原反应的电极,但注意,只有在电池放电时属于这种情况。
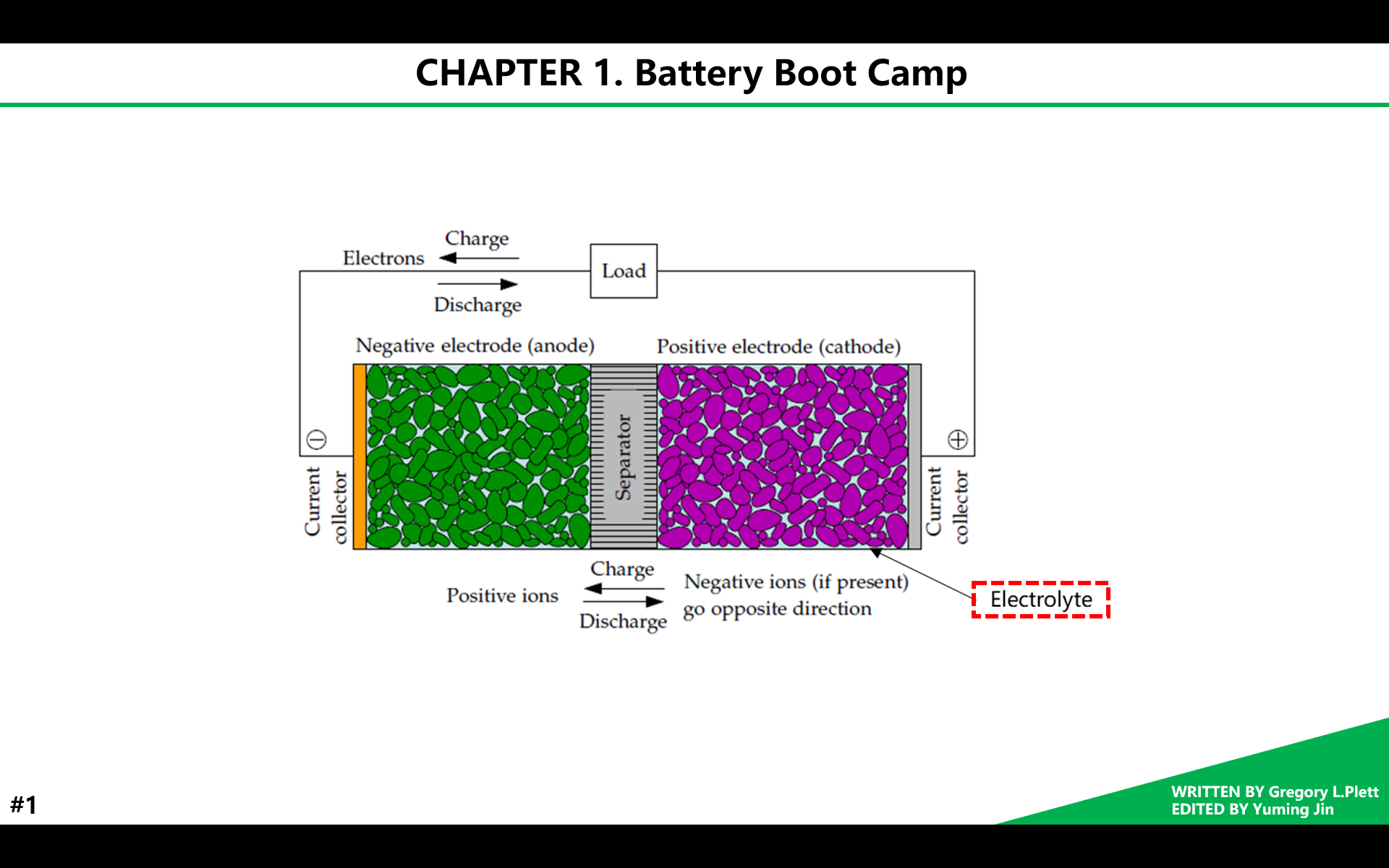
电解液是一种离子导体,为电极之间的内部离子电荷转移提供介质。电解液通常包括一种液体溶剂,和溶解其中的溶质,其中溶质可提供离子导电率,溶剂可为水或其他有机溶剂。放电时,阳离子向正极移动,阴离子向负极移动,充电时刚好相反。
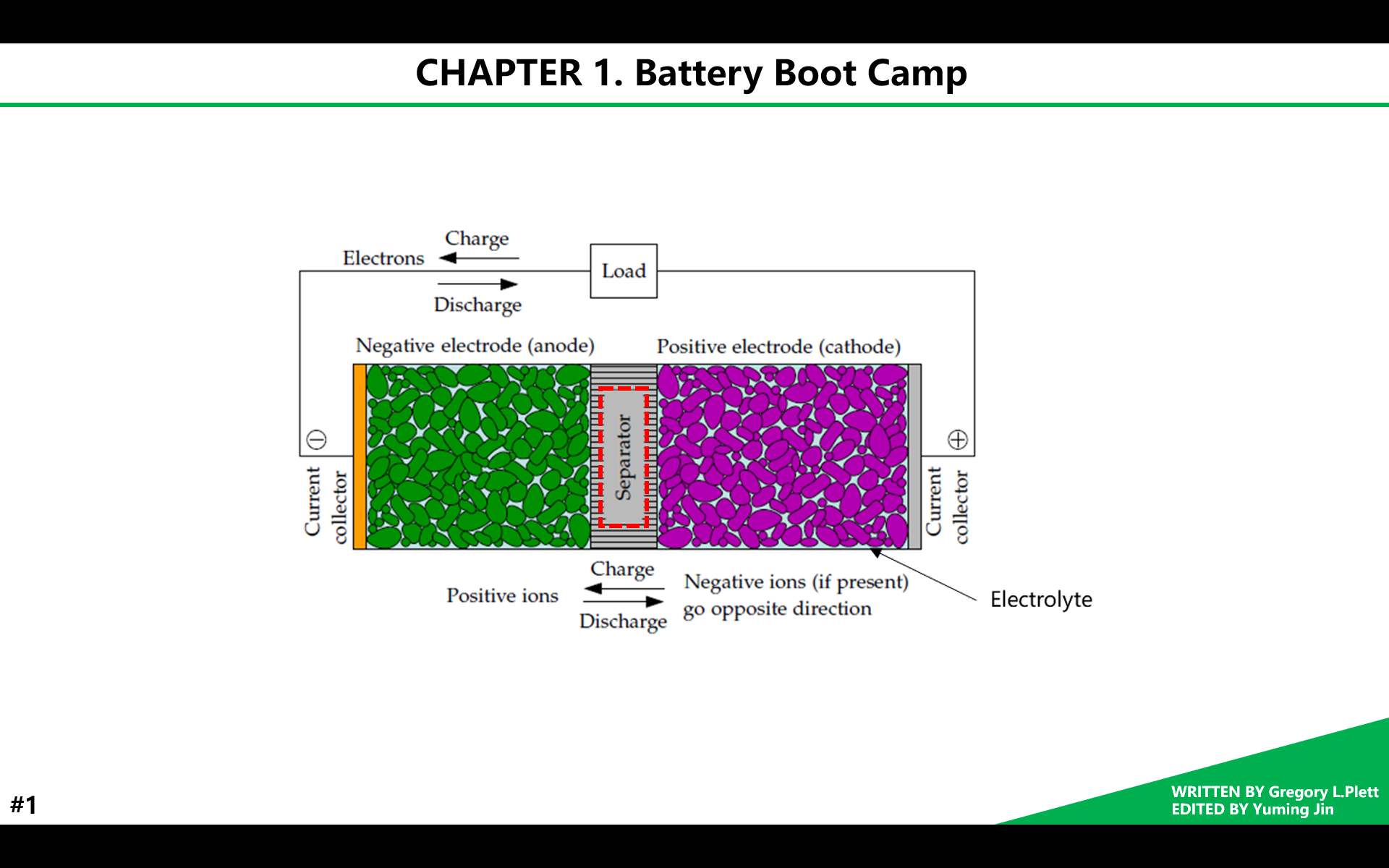
隔离膜从物理上隔绝了正负极,它既是一个离子导体,又是一个电子绝缘体。它的作用是防止正负极发生内部短路,从而避免电池单体的自放电甚至是热失控。
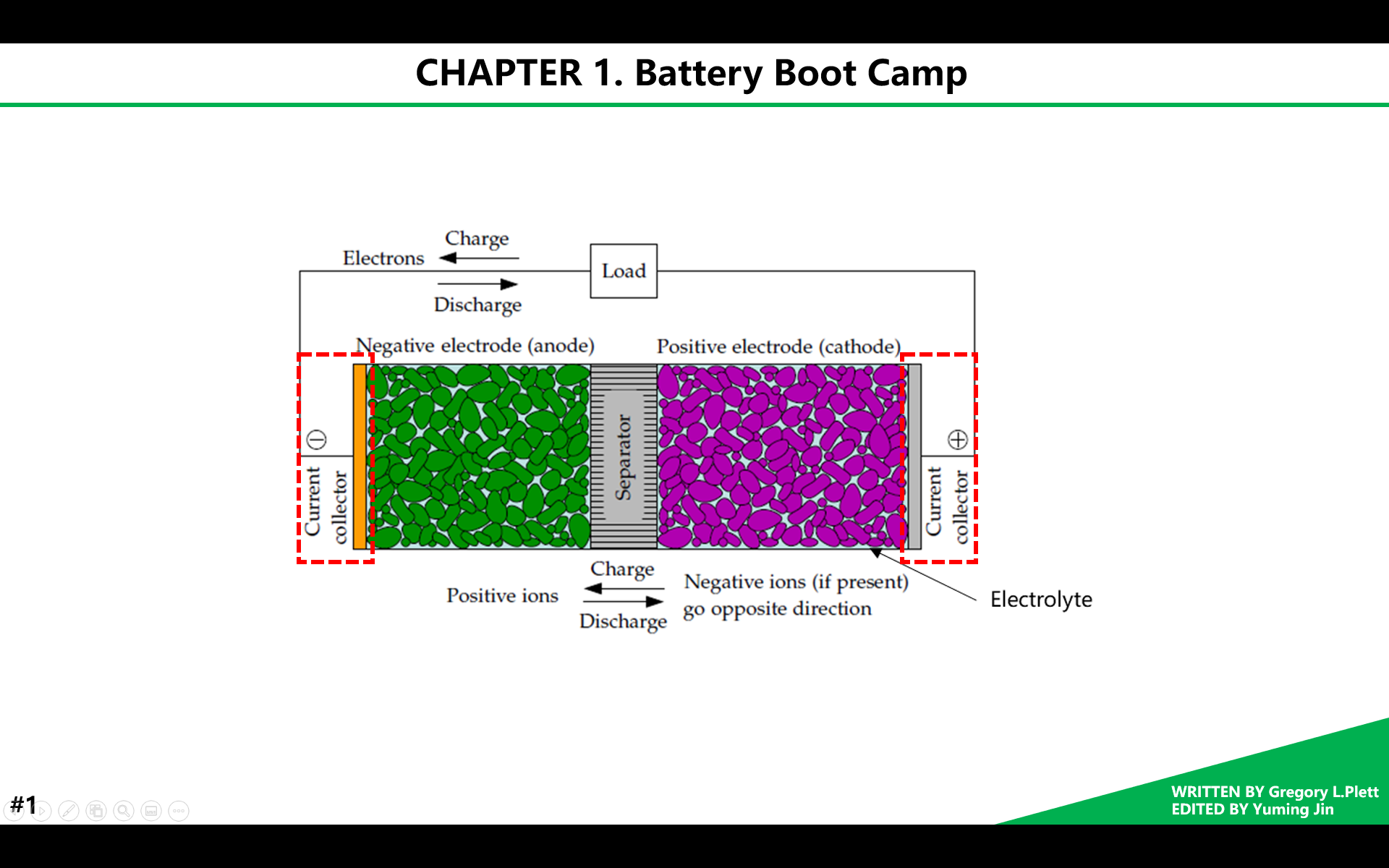
集流体是用于电子导通并承接正负极活性物质的,它不参与电化学反应,但允许简单的电子导通从而降低电极的电阻。例如,锂离子电池中通常用铜作为负极集流体,用铝作为负极集流体。
电池正负极端子间电压与正负极的材料种类相关,是正负极的电位差。
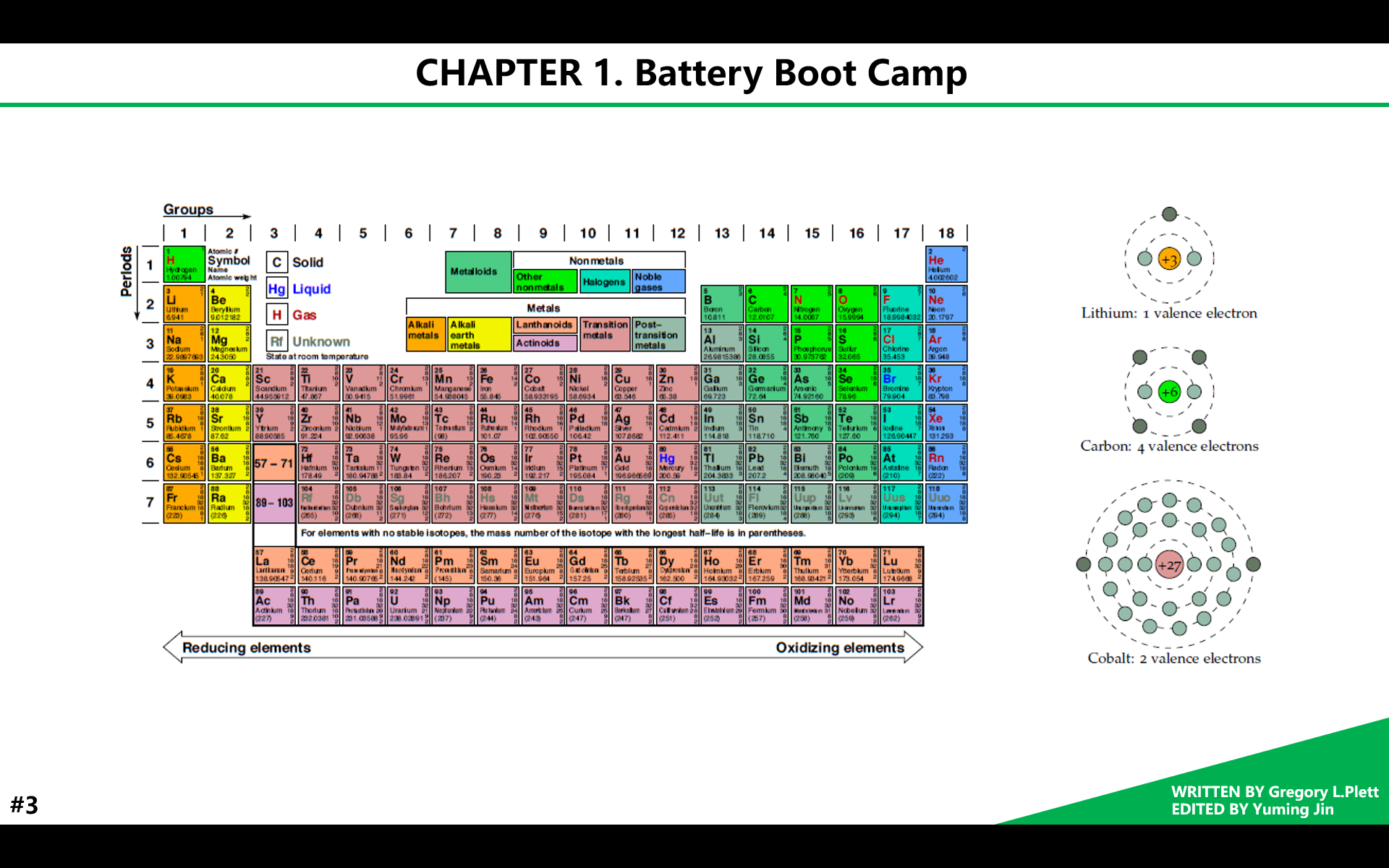
关于电位,我们通常把标准氢电极作为参比,将氢离子与电子生成氢气的半反应点位定义为0V。那么常见的电极半反应及对应电位可以看右边的列表:具有较低电位的化合物可作为负极,而较高电位的可作为正极。正负电极间的电位差越大,电压就越高。可以看到,表格中的锂具有最低的电位,表示它最容易被氧化。
那么如何更方便且全面地定性分析各元素的氧化或还原性呢?我们可以借助元素周期表,我想大家都不会陌生,尤其是化学专业的小伙伴,可能都经历过背诵全表的日子。通常我们习惯横向比较元素的氧化还原能力,从左向右,氧化性递增,反之,还原性递增。表中的每个格子对应一种元素,左上角标记了元素序数,及原子核中质子的数量;左下角为相对原子质量,基准是一个碳原子质量的十二分之一;右侧的一系列数字代表原子轨道中电子的排列数量,例如右侧的钴原子,核外共有27个电子,4个电子层,每层分别有2、8、15、2个电子。通常当原子最外层电子比次外层多1或2个电子时,电子更容易失去,形成正离子,此类原子还原性较强,例如周期表左侧第1、2列;反之,当原子最外层电子比次外层少1或2个电子时,电子更容易获得,形成负离子,此类原子氧化性较强,例如周期表右侧第2、3列。
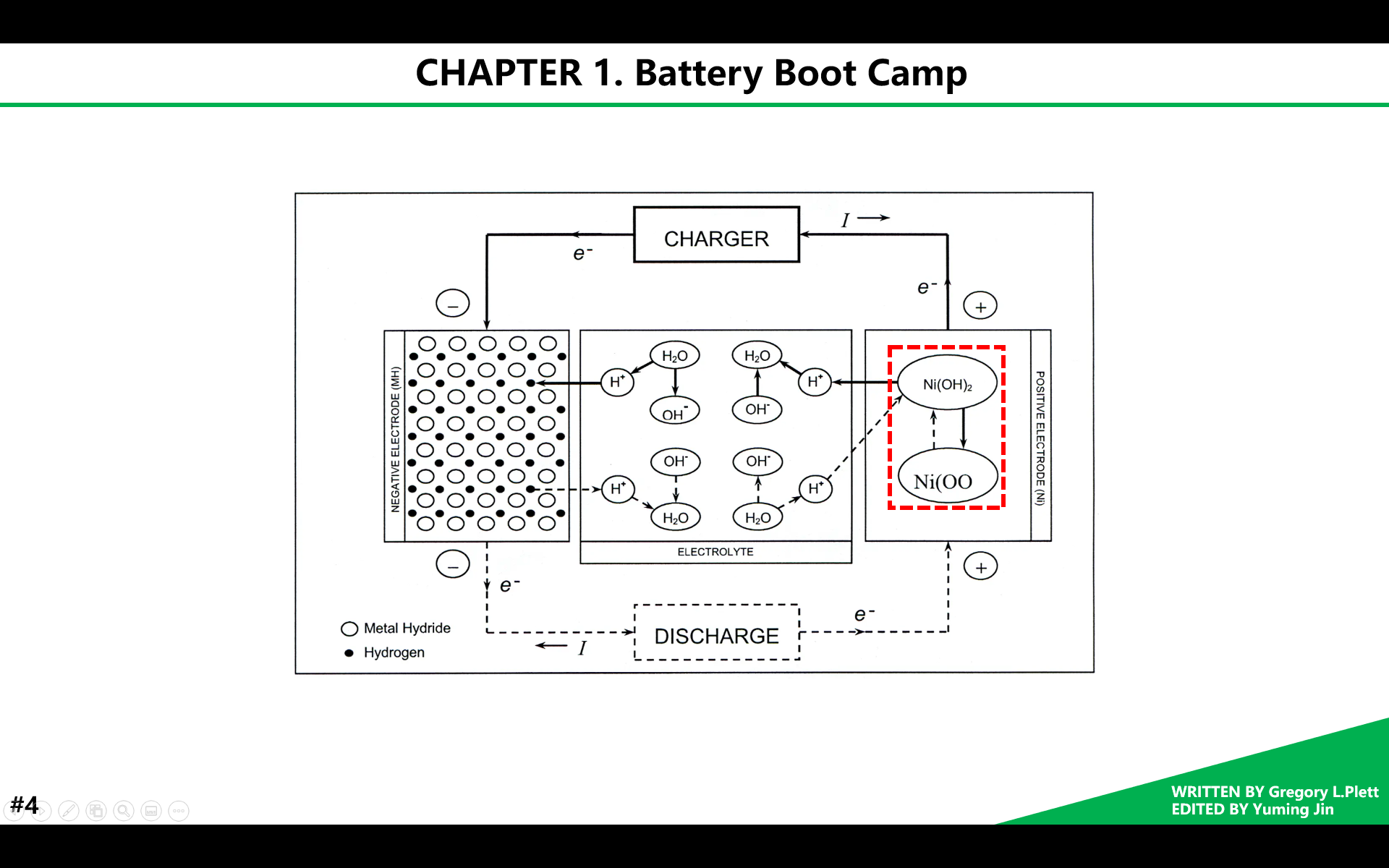
相对于传统的依靠氧化还原反应产生电压的一次电池,二次电池因其充放电过程可逆而得到更广泛地应用。例如镍氢电池,依靠金属镍吸附氢的同时不改变镍本身组分的特点而得到商用。
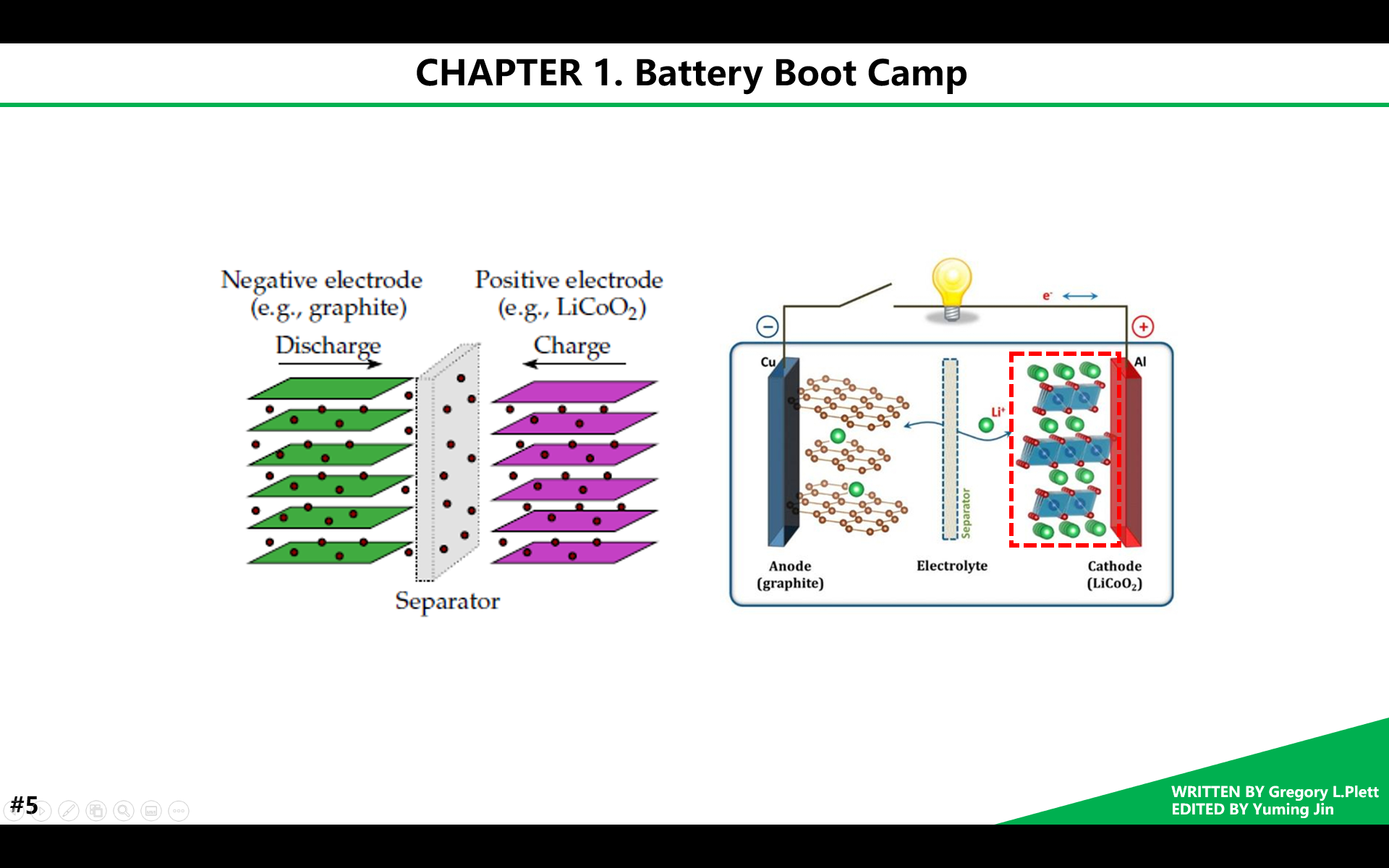
下面开始进入锂离子电池的部分。我们通常可以用左图形式描述一个锂离子电池:图中正负极被化成层状晶体结构,红色小球代表锂离子,可以在充放电过程中自由穿梭于层状结构之间。右图的电极材料表示更加直观,以钴酸锂化学体系为例,左边是负极石墨材料,右边是正极钴酸锂材料,其中锂是以电荷中性的形式独立存储的。每个锂原子的价电子是松散地分布在相邻原子周围的,这让我想起了固体物理和量子力学,电子的空间分布状态其实由它的概率密度函数决定,并不是宏观世界的粒粒可数的状态。正因为如此,锂没有被束缚在某一区域,而是可以自由移动的。锂在电极材料表面嵌入和脱出时,在开放的层状晶体结构内扩散,以平衡电极空穴内锂的浓度。充放电时,锂离子穿梭于正负极材料之间,类似一个摇椅,来回摇摆。因为这种嵌入脱出的方式比电化学反应温和很多,所以锂离子电池具有比其他二次电池更长的寿命。
直到现在,我们将锂电池电极看作质地均一的晶体块,然而微观世界中并非如此。实际上,电极是由数百万个电极颗粒构成的,这样可以增大电极的表面积,让锂离子更容易嵌入脱出,从而降低电池的整体阻抗,提高功率和容量。
例如左上角的图,是一个电池负极的局部扫描电镜照片,展示了不同尺度下石墨的形貌。
右上角是一个电池正极极的局部扫描电镜照片,展示了不同尺度下锰酸锂的形貌。可以看到与石墨材料的明显差异。
下方展示了电极的一个截面图,左边是刀片切开的面,右侧是聚焦离子束切开颗粒的过程,可以看到电极多孔的形貌。与一次电极材料混合在一起的是粘结剂,例如PVDF,还有一些导电添加剂,例如碳黑,用于提高电子导电性,这些添加剂是不具备电化学活性的。
好了,这就是本期视频的全部内容,下期我们将介绍锂电池的材料、生产工艺、失效模式等内容,敬请期待,我们下次再见,byebye!
 电池交流
电池交流 电池技术
电池技术 电池问答
电池问答 供求信息
供求信息 电池回收
电池回收 认证检测
认证检测 电池管理系统
电池管理系统 电池修复
电池修复 广告发布
广告发布 锂电池
锂电池 动力电池
动力电池 锂离子电池
锂离子电池 磷酸铁锂电池
磷酸铁锂电池 三元锂电池
三元锂电池 18650锂电池
18650锂电池 锂电池厂家
锂电池厂家 钠离子电池
钠离子电池 新能源汽车
新能源汽车 电池会议
电池会议 电池展会
电池展会 商务活动
商务活动